巨噬细胞研究热点及解决方案:免疫界“变形金刚”全景拆解!
Source: Elabscience®Published: 2025-08-26
巨噬细胞是单核吞噬细胞系统中的核心免疫细胞,在机体免疫防御、监视及内环境稳态维持中发挥关键作用。巨噬细胞在体内呈现出复杂且多样化的功能特征,包括:吞噬并清除细胞碎片、进行抗原提递以调节免疫应答、调节炎症反应及细胞因子分泌、促进组织修复与重塑,以及参与维持体内平衡的多层级信号通路调控网络。巨噬细胞的功能状态广泛参与多种疾病的发生与发展,包括癌症、自身免疫性疾病、心血管疾病、神经退行性疾病、代谢性疾病及创伤修复异常等。因此,靶向巨噬细胞调控策略已成为这些疾病领域中的重要研究方向。
一、巨噬细胞的起源与分类:高度异质性的“变形金刚”
巨噬细胞可分为胚胎来源的巨噬细胞和骨髓来源的巨噬细胞。胚胎来源的巨噬细胞在胚胎发育阶段就已定植于各个组织,如大脑中的小胶质细胞、肝脏中的库普弗细胞、皮肤中的朗格汉斯细胞等,这类细胞具有长期自我更新的能力,主要负责维持组织内的巨噬细胞的数量与稳态。而骨髓来源的巨噬细胞则来源于造血干细胞,经单核细胞阶段后进入血液循环,随后迁移到全身各组织,在局部微环境信号的诱导下进一步分化为成熟的巨噬细胞,主要参与应对感染、炎症及组织损伤修复等过程。
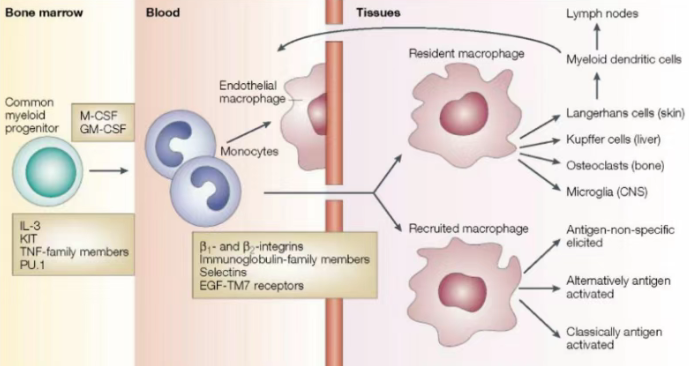
图1. 巨噬细胞的起源
二、巨噬细胞的激活和分化途径
巨噬细胞具有高度可塑性,其免疫功能取决于不同的激活状态与分化途径。CSF-1可诱导单核细胞分化为未活化的M0巨噬细胞。后者可在不同细胞因子的刺激下通过经典或非经典途径进一步极化为M1或M2型巨噬细胞。
M1 型巨噬细胞被认为是促炎表型,通常在LPS、IFN-γ等刺激下被激活,高表达MHC-Ⅱ和共刺激分子,释放大量的促炎细胞因子如TNF-α、IL-1β等,具有较强的吞噬和杀伤能力,在抗感染免疫中发挥重要作用。
M2型巨噬细胞则被视为抗炎和修复表型,主要由IL-4、IL-13等诱导活化,可进一步分为M2a、M2b、M2c和M2d四个亚型,该类细胞分泌IL-10等抗炎细胞因子,参与组织修复、血管生成以及免疫调节等过程。
需要注意的是,M1 和 M2 仅代表极化状态的两个极端,体内实际存在着大量介于两者之间的中间表型,它们的表型和功能随微环境信号动态变化,呈现高度可调的状态。
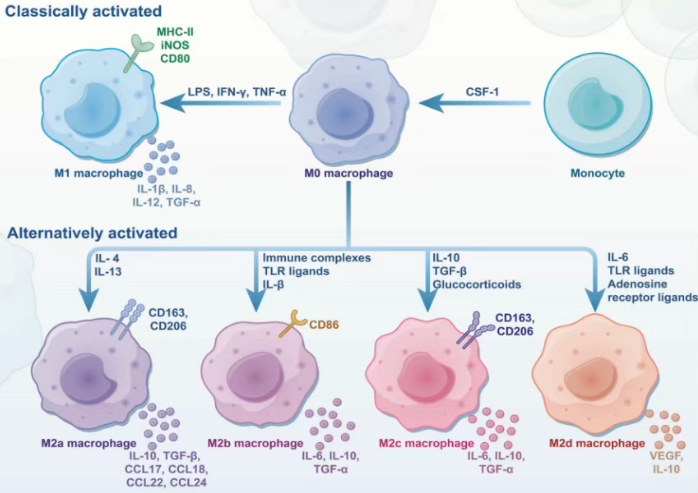
图2. 巨噬细胞的激活途径
三、M1/M2巨噬细胞代谢信号通路和免疫调节
巨噬细胞的免疫调节功能高度依赖于其细胞内代谢重编程。M1型巨噬细胞以有氧糖酵解为主要代谢特征,该过程促进乳酸积累,并伴随大量活性氧(ROS)和一氧化氮(NO)的生成。磷酸戊糖途径(PPP)为其提供还原型NADPH,进一步支持尿素循环(包括精氨酸合成及天冬氨酸-精氨酸琥珀酸分流途径,AASS)等过程。此外,三羧酸循环(TCA循环)中积累的代谢物(如柠檬酸和琥珀酸)不仅参与脂肪酸代谢要,还能通过稳定缺氧诱导因子-1α(HIF-1α),促进促炎基因及糖酵解相关基因的转录与表观遗传学调控。
相比之下,M2型巨噬细胞则主要依赖氧化磷酸化(OXPHOS)及氧化状态的TCA循环以高效产生ATP。其代谢特征包括精氨酸代谢、β-氧化和谷氨酰胺分解,为抗炎及修复功能提供能量和生物合成前体。
值得注意的是,多种代谢途径通过其关键中间产物或终产物参与免疫信号的调节:有氧糖酵解产物(如乳酸)、一氧化氮、脂肪酸合成以及谷氨酰胺代谢均发挥重要作用;TCA循环中间体(如乙酰辅酶A、柠檬酸、衣康酸和琥珀酸)亦是重要的免疫调节分子;同时,关键代谢酶(如己糖激酶2 (HK-II)、3-磷酸甘油醛脱氢酶 (GAPDH) 和精氨酸酶1 (Arg1))等也在免疫调节中扮演关键角色。
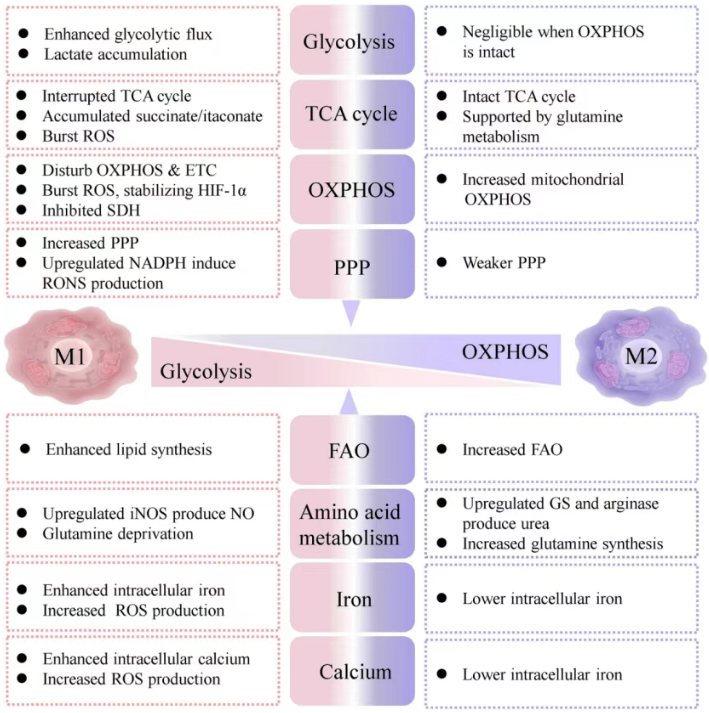
图3. M1/M2型巨噬细胞差异性代谢
四、巨噬细胞的生物功能:从免疫防御到系统稳态的“多面手”
1. 免疫防御:吞噬、抗原呈递与炎症调控
-
吞噬作用:巨噬细胞通过表面模式识别受体(PRRs,如Toll样受体和甘露糖受体)识别病原体或凋亡细胞,经吞噬作用形成“吞噬溶酶体”以降解目标物。例如,当中性粒细胞死亡后释放的“中性粒细胞胞外陷阱(NETs)”后,巨噬细胞可及时清除这些细胞,避免过度炎症反应发生。
-
抗原呈递:巨噬细胞处理抗原后通过MHC II类分子将抗原肽呈递给CD4+ T细胞,从而激活适应性免疫。该机制在抗胞内病原体(如结核分枝杆菌)感染过程中尤为关键。
-
炎症调控:M1型巨噬细胞通过分泌IL-1β、IL-6等促炎因子增强炎症反应;M2型巨噬细胞则通过释放IL-10、TGF-β等抗炎因子抑制过度炎症,并促进组织修复。两者形成动态平衡,若这一“双向调节”机制失衡,可能引发慢性炎症(如类风湿关节炎)或肿瘤微环境中的免疫抑制状态。
2. 组织修复与重塑:从“清道夫”到“建筑师”
在组织发生损伤(如心肌梗死或皮肤创伤)后,巨噬细胞通过多种机制协同促进修复过程:
-
清除坏死组织:在损伤早期,以M1型为主的巨噬细胞记录吞噬死亡细胞和碎片,有效抑制炎症进一步扩散。
-
促进血管新生:巨噬细胞分泌VEGF、PDGF等生长因子,招募内皮细胞并促进形成新血管生成,为组织修复提供营养与氧气支持。
-
调控细胞外基质重塑:通过分泌基质金属蛋白酶(MMPs)降解受损细胞外基质(ECM),并释放TGF-β等因子激活成纤维细胞,促进胶原合成与组织结构重建。
值得注意的是,如果修复反应过度或者失控,巨噬细胞持续分泌TGF-β并激活肌成纤维细胞,可能导致病理性纤维化发生,如在肝纤维化或肺纤维化中所见。
3. 代谢调控:连接免疫与代谢的“桥梁”
巨噬细胞深度参与全身代谢稳态:
-
铁循环:巨噬细胞通过铁转运蛋白(Ferroportin)介导铁离子释放,供给红细胞生成所需;在感染状态下,则通过铁螯合策略限制病原体对铁的利用,形成“营养免疫”效应。
-
胆固醇代谢:肝脏中的库普弗细胞通过清道夫受体SR-A和CD36摄取氧化低密度脂蛋白(ox-LDL),转化为泡沫细胞,进而促进动脉粥样硬化斑块形成。
-
能量平衡:脂肪组织巨噬细胞(ATMs)在肥胖状态下被激活,分泌TNF-α和IL-6等炎症因子,这些因子干扰胰岛素信号,促进脂肪分解增强并引发全身性胰岛素抵抗。
4. 肿瘤微环境中的双重角色:敌人还是盟友?
肿瘤相关巨噬细胞(TAM)是肿瘤微环境(TME)中含量最丰富的免疫细胞,约占其免疫细胞总数的30%-50%,具有高度异质,通常可分为以下两类:
-
促肿瘤表型(M2-like TAM):占TAM多数,通过分泌VEGF、EGF等因子促进肿瘤血管生成与侵袭;通过分泌CCL22招募调节性T细胞(Treg),从而抑制抗肿瘤免疫;还可分泌MMPs降解基底膜,促进肿瘤转移。
-
抗肿瘤表型(M1-like TAM):所占比例较低,主要通过吞噬肿瘤细胞、递呈抗原激活CD8+T细胞,发挥抗肿瘤免疫作用。
近年来研究显示,TAM的表型受肿瘤细胞来源的CSF-1(巨噬细胞集落刺激因子)、TGF-β等关键因子调控,针对TAM极化的干预政策已成为肿瘤治疗领域的重要研究方向。
五、巨噬细胞的研究思路和当前热点
1、巨噬细胞代谢重编程与肿瘤免疫治疗
-
研究思路:
肿瘤相关巨噬细胞(TAMs)具有高度可塑性,其功能受肿瘤细胞分泌因子(如CSF-1、IL-4)调控。最新研究探索通过靶向TAMs的信号通路(如CSF-1R、CD47-SIRPα)来重编程TAMs,使其从促肿瘤表型转化为抗肿瘤表型。
-
技术实现路径:
✔代谢组学分析或多组学分析;
✔临床数据分析;
✔体内体外实验模型搭建及检测(信号通路测试、代谢通路测试等)。
2、巨噬细胞与神经退行性疾病
-
研究思路:
巨噬细胞(小胶质细胞)在中枢神经系统(CNS)中发挥双重作用,既可清除神经毒性物质,也可能引发神经炎症。最新研究关注通过调控小胶质细胞的代谢和表型,延缓阿尔茨海默病、帕金森病等神经退行性疾病的进展。
-
技术实现路径:
✔蛋白组学分析/代谢组学分析(神经损伤关键蛋白标记物发现等);
✔超分辨显微技术/PET成像技术(关键蛋白沉积检测);
✔信号通路检测-体内/体外模型建立及检测。
3、巨噬细胞与心血管疾病
-
研究思路:
① 极化动态与表观遗传调控:单核细胞来源的CCR2+巨噬细胞和胚胎源性CCR2-巨噬细胞的极化对于炎症和纤维化的调控受多种因子影响。
② 细胞间交互网络:巨噬细胞-成纤维细胞轴的转化调节促进心室重构;
③ 代谢重编程与功能转换:M1巨噬细胞的糖酵解代谢途径缓解心肌缺血再灌注损伤;巨噬细胞脂肪酸氧化与修复代谢途径促使向修复表型转化,增强心肌梗死后血管生成。
-
技术实现路径:
✔多组学分析(确定关键因子);
✔临床代谢数据分析及代谢组学分析;
✔体内体外实验模型搭建及检测(信号通路测试、代谢通路测试等)。
4、巨噬细胞与代谢性疾病
-
研究思路:
肥胖、糖尿病等代谢性疾病中,巨噬细胞在脂肪组织中的浸润和极化异常与胰岛素抵抗密切相关。最新研究关注通过调控巨噬细胞的代谢和功能,改善胰岛素敏感性。
-
技术实现路径:
✔代谢组学分析(确定关键影响因子)或临床数据统计分析(确定关键代谢因子,如酶或代谢产物);
✔体内体外模型建立;
✔代谢微环境免疫细胞检测;
✔代谢通路相关指标检测及影响机制验证分析。
5、巨噬细胞与衰老
-
研究思路:
衰老过程中,巨噬细胞的功能逐渐衰退,导致慢性炎症和免疫监视能力下降。最新研究探索通过调控巨噬细胞的代谢和功能,延缓衰老相关疾病的发生。
-
技术实现路径:
✔体内体外模型建立;
✔免疫微环境检测和巨噬细胞分化及功能检测;
✔衰老关键指标相关通路检测验证衰老机制。
6、巨噬细胞与自身免疫疾病调节
-
研究思路:
巨噬细胞在自身免疫性疾病(如类风湿性关节炎、系统性红斑狼疮)中发挥促炎作用。最新研究关注通过调控巨噬细胞的极化状态(如抑制M1型极化)来减轻炎症反应。
-
技术实现路径:
✔体内体外模型建立;
✔巨噬细胞极化状态及功能检测;
✔药物或影响因子治疗效果或影响效果检测验证调节机制。
7、巨噬细胞与药物治疗
-
研究思路:
纳米药物和巨噬细胞工程化改造:利用纳米技术(如纳米颗粒、纳米载体)将药物或基因靶向递送至巨噬细胞,增强治疗效果或通过基因编辑技术(如CRISPR/Cas9)或合成生物学手段,改造巨噬细胞的功能,使其表达特定的受体(如CAR-M)或分泌治疗性因子。
-
技术实现路径:
✔体内体外模型建立;
✔靶向药物设计和体内体外药理药效分析和验证。
六、巨噬细胞研究的系统化解决方案
基于巨噬细胞热门研究内容,常见的细胞模型及其检测解决方案如下所示:
(1)基础功能研究模型
|
模型类型 |
制备方法 |
检测指标 |
应用场景 |
|
原代巨噬细胞(BMDM) |
小鼠骨髓单核细胞经M-CSF(10-20 ng/mL)培养7天,贴壁后纯度>90% |
流式(CD68、CD86、CD206)、吞噬实验(荧光标记病原体)、qPCR(iNOS、Arg1) |
基础吞噬功能、极化机制研究 |
|
腹腔巨噬细胞 |
腹腔灌洗法收集小鼠腹腔巨噬细胞,PBS洗涤后重悬于RPMI-160培养基 |
流式(F4/80、MHC-II)、ELISA(TNF-α、IL-6) |
炎症模型、急性感染研究 |
|
M1型极化模型 |
THP-1细胞经PMA(100-200 ng/mL)分化24 h后,用LPS(1 μg/mL)+ IFN-γ(20 ng/mL)刺激24 h;或Raw264.7细胞用LPS(1 μg/mL)+ IFN-γ(20 ng/mL)刺激24 h |
流式(CD86、CD40)、qPCR(TNF-α、IL-1β)、ROS检测 |
促炎反应、感染免疫研究 |
|
M2型极化模型 |
THP-1细胞经PMA(100-200 ng/mL)分化24 h后,经IL-4(20-50 ng/mL)或IL-13(20-50 ng/mL)处理48 h;Raw264.7细胞经IL-4(20-50 ng/mL)或IL-13(20-50 ng/mL)处理48 h |
流式(CD206、CD163)、Western Blot(Arg1、TGF-β)、代谢组学(脂肪酸氧化) |
抗炎修复、肿瘤微环境研究 |
(2)疾病特异性研究模型
|
模型名称 |
制备方法 |
检测指标 |
应用场景 |
|
TAMs共培养模型 |
巨噬细胞与肿瘤细胞(如4T1乳腺癌细胞)按1:5比例共培养,模拟肿瘤微环境 |
流式(TGF-β、IL-10)、活体成像(肿瘤体积)、代谢组学(乳酸/谷氨酰胺) |
肿瘤免疫逃逸、靶向治疗评估 |
|
泡沫细胞模型 |
THP-1巨噬细胞经Ox-LDL(80 mg/L)处理48 h,油红O染色鉴定脂质沉积 |
qPCR(ABCA1、CD36)、脂质组学(胆固醇酯含量)、免疫荧光(Mac-2) |
动脉粥样硬化的斑块稳定性测试、降脂药物筛选 |
|
博来霉素诱导模型 |
小鼠气管滴注博来霉素(5 mg/kg),分离肺组织巨噬细胞 |
Masson染色、α-SMA免疫组化、TGF-β1、Smad3通路激活检测 |
肺纤维化疾病中抗纤维化药物疗效评估 |
|
压力超负荷模型 |
小鼠主动脉缩窄术,分离心脏组织巨噬细胞 |
心脏超声(LVEF)、免疫组化(CD68+TUNEL双染)、代谢组学(脂肪酸、葡萄糖) |
心肌肥大等疾病中,心肌修复、代谢重编程干预研究 |
|
高脂饮食诱导模型 |
C57BL/6小鼠喂食60%高脂饲料12周,分离附睾脂肪组织巨噬细胞 |
流式(M1/M2比例)、ROS水平、葡萄糖摄取实验 |
肥胖相关糖尿病的胰岛素抵抗、抗炎药物开发 |
|
CCl4诱导肝纤维化模型 |
小鼠腹腔注射CCl4(2 mL/kg,每周2次)12周,分离Kupffer细胞 |
肝功能检测(ALT、AST)、油红O染色、NLRP3炎症小体激活 |
非酒精性脂肪肝的肝保护药物、代谢调控研究 |
|
脓毒症模型 |
小鼠盲肠结扎穿刺术(CLP),分离腹腔巨噬细胞 |
血浆IL-6、TNF-α水平、组织病理评分(肺、肾损伤)、外泌体miRNA谱分析 |
败血症的抗炎治疗、免疫调节剂筛选
|
巨噬细胞作为免疫系统的核心组成部分,因其极度的可塑性和多功能性,已成为当今生物医学研究的热点之一,想要更深入“拿捏”它们?别走开!9月份我们将陆续推出以下内容:组织驻留巨噬细胞检测宝典、巨噬细胞代谢研究攻略以及巨噬细胞M1/M2定向极化秘籍和检测方案。
Elabscience®致力于为大家呈现精彩的实验成果,包括形态学观察、细胞内代谢途径分析以及细胞免疫特征的检测。更多硬核干货,持续锁定Elabscience®推文,也欢迎在留言区和我们交流你的实验心得哦~
引用文献:
[1] Guan F , Wang R , Yi Z ,et al.Tissue macrophages: origin, heterogenity, biological functions, diseases and therapeutic targets[J].Signal Transduction and Targeted Therapy[2025-07-31].DOI:10.1038/s41392-025-02124-y.
[2] Gordon S. Alternative activation of macrophages. Nat Rev Immunol. 2003;3(1):23-35. doi:10.1038/nri978
[3] Wang LX, Zhang SX, Wu HJ, Rong XL, Guo J. M2b macrophage polarization and its roles in diseases. J Leukoc Biol. 2019 Aug;106(2):345-358. doi: 10.1002/JLB.3RU1018-378RR. Epub 2018 Dec 21. PMID: 30576000; PMCID: PMC7379745.
[4] Guan F , Wang R , Yi Z ,et al.Tissue macrophages: origin, heterogenity, biological functions, diseases and therapeutic targets[J].Signal Transduction and Targeted Therapy[2025-07-31].DOI:10.1038/s41392-025-02124-y.
[5] Gordon S. Alternative activation of macrophages. Nat Rev Immunol. 2003;3(1):23-35. doi:10.1038/nri978.
[6] Wang LX, Zhang SX, Wu HJ, Rong XL, Guo J. M2b macrophage polarization and its roles in diseases. J Leukoc Biol. 2019 Aug;106(2):345-358. doi: 10.1002/JLB.3RU1018-378RR.
[7] Fujiyama S , Nakahashi-Oda C , Abe F ,et al.Identification and isolation of splenic tissue-resident macrophage sub-populations by flow cytometry.[J].Int Immunol, 2019(1).DOI:10.1093/intimm/dxy064.
[8] Meng T , He D , Han Z ,et al.Correction: Nanomaterial-Based Repurposing of Macrophage Metabolism and Its Applications[J].Nano-Micro Letters, 2024, 16(1).DOI:10.1007/s40820-024-01491-5.






